J. Phys. Chem. B. にイソペンテニル二リン酸のリン酸化関与する IPK の QM/MM 計算の論文が出ていましたので、簡単に紹介します。
“Reaction Mechanism of Isopentenyl Phosphate Kinase: A QM/MM Study”
James McClory, David J. Timson, Warispreet Singh, Jian Zhang, & Meilan Huang
J. Phys. Chem. B. in press.
概要
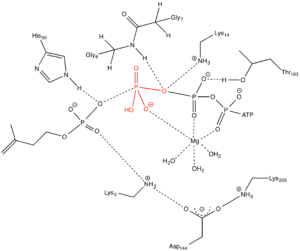
イソペンテニルリン酸キナーゼ(IPK)は、Mg![]() と ATP 依存的なリン酸化反応を触媒する酵素である。イソペンテノール類の合成における重要な前駆体であるイソペンテニル二リン酸の生成に関与している。しかし、ATP 複合体の IPK の結晶構造において二価金属イオンの位置は決定されていないため、IPの触媒メカニズムには未だ不明瞭な点があり、その結果バイオ燃料や医薬品設計を目的としたエンジニアリングの妨げとなっている。本論文では、触媒的に金属イオンのMg
と ATP 依存的なリン酸化反応を触媒する酵素である。イソペンテノール類の合成における重要な前駆体であるイソペンテニル二リン酸の生成に関与している。しかし、ATP 複合体の IPK の結晶構造において二価金属イオンの位置は決定されていないため、IPの触媒メカニズムには未だ不明瞭な点があり、その結果バイオ燃料や医薬品設計を目的としたエンジニアリングの妨げとなっている。本論文では、触媒的に金属イオンのMg![]() との複合体を作成し、MD シミュレーションと QM/MM (B97d/AMBER99)を用いた計算を行い、リン酸化反応機構の解明を行った。
との複合体を作成し、MD シミュレーションと QM/MM (B97d/AMBER99)を用いた計算を行い、リン酸化反応機構の解明を行った。
また、基質が結合した状態と結合していない状態を比較したところ、αGヘリックス上に位置している Lys204、Glu207、および Lys211 が大きく変化することがわかった。コンフォメーション変化により αG ヘリックス上の残基と Asp145 が強い salt bridge を形成する。また、これにより、SER142 をテザーする。さらに、コンフォメーション変化により、αGとαEヘリックスの間にある基質の入り口が閉鎖される。計算の結果、リン酸化反応の活性化エネルギーは
17.58kcal/mol であり、これまでの実験的なキネティクスのデータと一致した。また、グリシンが豊富である、非常に保存されたループ領域である Gly8 が、Lys14と共に遷移状態構造を安定化することも明らかにした。
計算手法
Thermoplasma acidophilum (THA) 由来の IPK の結晶構造 (PDB: 3LKK) が計算に用いられました。FomA (PDB Code: 3QUN)というホモログ酵素を参考に、Mg![]() は手動で置かれたそうです。重要な残基のプロトン化状態の判断は、proPka server を用いて行ったようです。
は手動で置かれたそうです。重要な残基のプロトン化状態の判断は、proPka server を用いて行ったようです。
MD シミュレーションは AMBER14 で行っています。ATP とイソペンテニルリン酸は HF/6-31g(d) で RESP charge を計算したようです。TIP3P water box で水分子を付与しました。変異体酵素については Discovery Studio を使用したそうです。
QM/MM は gaussian09 で ONIOM を用いて行っています。QM 部分は B97D/6-31G(d)、MM 部分は Amber Parm99。
内容
IPK は、amino acid kinase (AAK) superfamily に属する酵素であり、![]() のサンドイッチ構造を特徴としています。IPP の生合成はメバロン酸経路で行われていますが、この経路では計 5 つのリン酸化酵素の結晶が報告されていますが、IPP 以外の他の 4 つのリン酸化酵素はリン酸結合ループ(P-loop)を構造的な特徴としてもつ GHMP family に属しています。
のサンドイッチ構造を特徴としています。IPP の生合成はメバロン酸経路で行われていますが、この経路では計 5 つのリン酸化酵素の結晶が報告されていますが、IPP 以外の他の 4 つのリン酸化酵素はリン酸結合ループ(P-loop)を構造的な特徴としてもつ GHMP family に属しています。
結晶構造中で Mg![]() の正確な位置が分からなかったということで、今回の論文では Mg
の正確な位置が分からなかったということで、今回の論文では Mg![]() の位置を QM/MM で決めたという点が一つめのポイントになります。
の位置を QM/MM で決めたという点が一つめのポイントになります。
計算の結果、His50 が基質のリン酸基に結合していることがわかり、リン酸化反応において重要な残基であることがわかりました。Thr163 は ATP のフレキシブルな構造部分と結合することにより、間接的に反応を促進しているようです。
また、概要の所にも書いてありますが、αGヘリックス上に位置している Lys204、Glu207、および Lys211 が基質の結合に際して大きく動くことがわかりました。このコンフォメーション変化により αG ヘリックス上の残基と Asp145 が強い salt bridge を形成し、これにより Ser142 をテザーします。さらに、コンフォメーション変化により、αGとαEヘリックスの間にある基質の入り口が閉鎖されることもわかりました。
さらに、よく保存されている領域である Gly8 や Lys14 が遷移状態を安定化していることも計算により示されています。
この論文、座標データが一切載っていないんですが、いいのでしょうか?この論文以外にも、時折計算の論文で座標が載っていない論文ありますが、良いのでしょうか?Figure とかエネルギーとかいくら見せられても、それだけでは信じられないのですが。。。
また、考察に関しても計算によって得られた構造を説明しているだけで、反応駆動力の説明など有機化学的な考察はありませんでした。。。
関連する記事
- ニューラルネットワークを利用した粗視化シミュレーション コンフォメーション探索
- Threadripper 並列化効率改善?【gaussian16】
- Threadripper Gaussian16 ベンチマーク
- Threadripper 自作 PC 組み立て編【AMD】
- IRC 計算がうまくいかない時
- スピン状態依存的な光環化反応の計算
- Threadripper 正式発表【8月発売予定】
- 【Gaussian 16】デスクトップ PC で並列計算する際の注意点【Hyperthreading】
- スパコンランキング発表!日本はGREEN500上位独占!【2017年6月】
- 【AMD_Naples】正式名称はEPYCに決定!クロック数は2.8 GHz【基本スペックなど】
- GPU を用いた並列計算
- 自作 PC をつくってみた!
- Fedora25 に nVIDIA のドライバーをインストール
- 自作 PC を作ってみた!【OS 編】