1,2-ヒドリド移動反応は、有機化学の教科書や論文などで、カルボカチオンの項に登場します。
実際に、インターネットで「ヒドリドシフト」と検索すると、こちらの資料やこちらのテストが検索上位に来ます。これらの資料内では、基質にカルボカチオンが生じたのちに、 1,2-ヒドリドシフトが進行する反応経路が示されています。
学会等のディスカッションでも、「ヒドリドシフト」という言葉はよく聞かれるもので、一般的に受け入れられているものです。
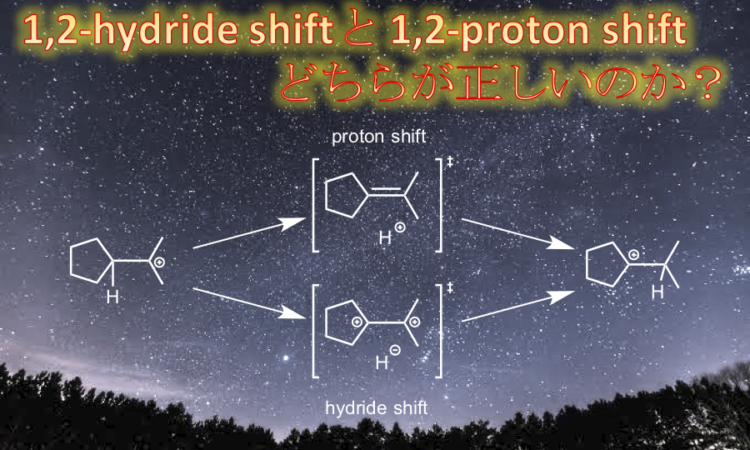
しかし、「1,2-ヒドリドシフト」は間違いであり、正しくは「1,2-プロトンシフト」であるという計算結果が示されています。
目次
DFT 計算は 1,2-プロトンシフトを支持
もともと分子内プロトンシフトは、Croteau らのTaxadiene 生合成の研究で提唱されました。
“Intramolecular proton transfer in the cyclization of geranylgeranyl diphosphate to the taxadiene precursor of taxol catalyzed by recombinant taxadiene synthase”
David C Williams, Brian J Carroll, Qingwu Jin, Christopher D Rithner, Steven R Lenger, Heinz G Floss, Robert M Coates, Robert M Williams & Rodney Croteau
Chemistry & Biology 2000, 7, 969–977.
DOI: 10.1016/S1074-5521(00)00046-6
その後、UC Davis の Dean Tantillo らが DFT 計算を行い、ヒドリドシフトではなくプロトンシフトの方が有利であるとの計算結果を示しております。
“Which Is More Likely in Trichodiene Biosynthesis: Hydride or Proton Transfer? “
Young J. Hong & Dean J. Tantillo*
Org. Lett. 2006, 8, 4601–4604.
DOI: 10.1021/ol061884f
なぜプロトンシフトなのか?〜遷移状態構造(TSS)を考察〜
では、なぜプロトンシフトの方が有利なのでしょうか?
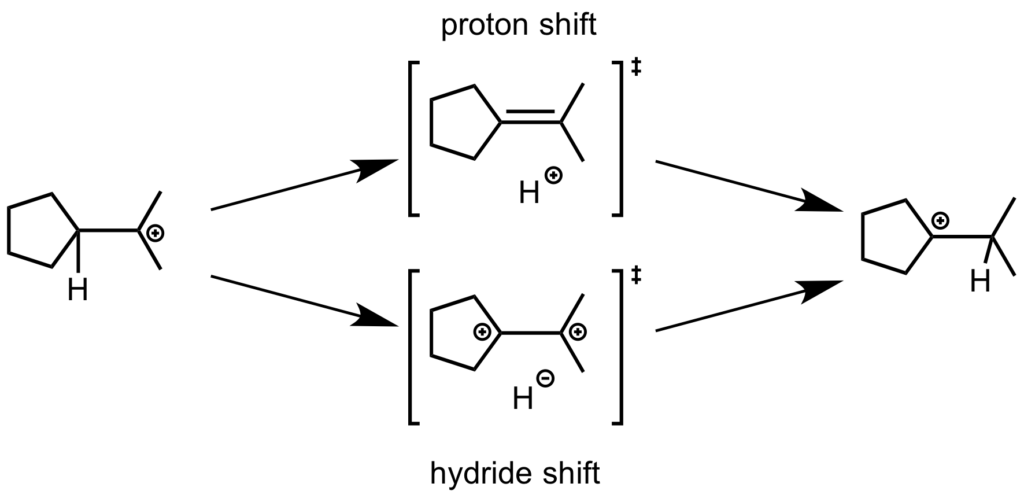
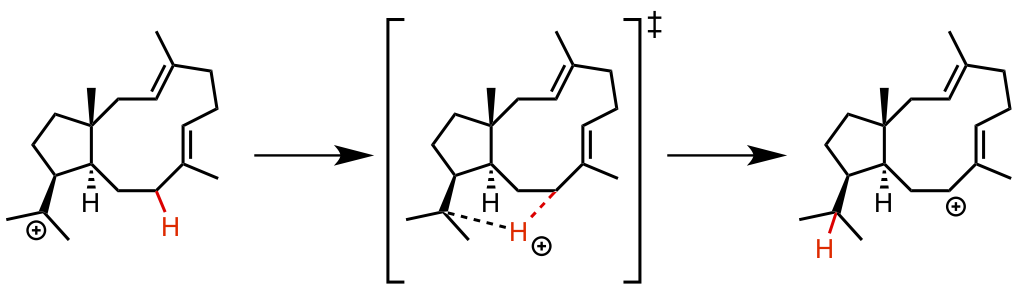
1,2-水素移動反応の遷移状態構造をヒドリドとプロトン移動の両方で考えてみましょう。
上図に示すように、ヒドリドシフトの場合は隣接する炭素上にカチオンが発生した C–C 単結合とヒドリドの組み合わせという遷移状態構造になります。
一方で、プロトンシフトの場合は、C=C 二重結合上をプロトンが滑るように移動するという、極めて安定な遷移状態構造になります。
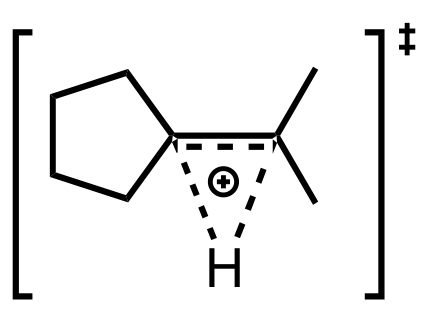
また、プロトンシフトの遷移状態構造をより正確に記述すると、三中心二電子結合様の構造が生じ、全体として非常に安定化されていることがわかると思います。
プロトンの空軌道に C=C の ![]() 電子が入ることにより安定化が起きます。
電子が入ることにより安定化が起きます。
テルペン生合成では、C–H ![]() 相互作用によって 1,2-水素移動が加速するという例が散見されますが、これも芳香環の
相互作用によって 1,2-水素移動が加速するという例が散見されますが、これも芳香環の ![]() 電子がプロトンを安定化することによって生じるものです。
電子がプロトンを安定化することによって生じるものです。
参考: C–H π 相互作用で 1,2-H shift を加速
少し話が逸れてしまいましたが、プロトンシフトが有利であるということは、DFT 計算の結果のエネルギー値を見るまでもなく、当たり前であると思います。
このように、遷移状態構造を交えて有機化学的に説明されると非常に当たり前のことのように感じます。実際に NBO 計算電荷を見てみても、移動する水素はヒドリドではなく、プロトンなのですが、多くの人がこの反応のことを 1,2-ヒドリドシフトと呼んでいます。
プロトンシフトの考え方がまだ浸透していない面もあることから、いくつかの文献では、1,2-hydrogen shift (1,2-水素移動反応)と、無駄な議論を避ける書き方を採用しているようです。
1,2 水素移動 vs 1,3 水素移動
ヒドリドシフトではなく、プロトンシフトが正しいと言うと、また重箱のすみをつつくようなことを…と感じる方も知るかもしれませんね。
しかし、正しい知識を持つことで、正確な反応機構を提唱することが出来ます。
その一例が、東京大学のグループが発表したジテルペン化合物 Cyclooctatin の生合成反応機構です。
“Cation-Stitching Cascade”: exquisite control of terpene cyclization in cyclooctatin biosynthesis.
Sato, H., Teramoto, K., Masumoto, Y., Tezuka, N., Sakai, K., Ueda, S., Totsuka, Y., Shinada, T., Nishiyama, M., Wang, C., Kuzuyama, T. & Uchiyama, M.
Sci. Rep. 2015, 5, 18471.
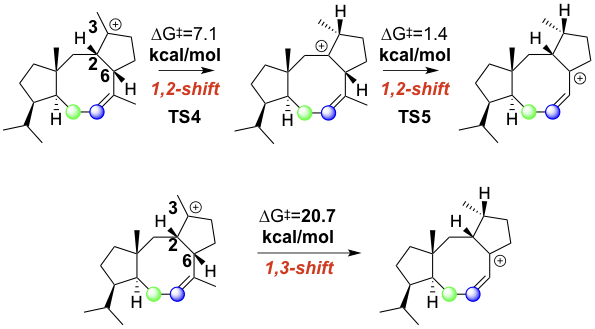
詳細は省略しますが、当初 Cyclooctatin の生合成経路では、 5 員環上での 1,3 ヒドリドシフトが想定されていました(図 3 下段)。
しかしながら、DFT 計算を行うと、1,3 ヒドリドシフトではなく、1,2-プロトンシフトを二回繰り返す方が有利であるという結果が示されました(図3上段)。
この要因については、
- 1,2-プロトンシフトでは、三中心二電子結合様の構造により TS が非常に安定化されるため。
- 5 員環上での 1,3-水素移動反応は、遷移状態構造で 5 員環が湾曲する必要があり、エネルギー的に不利である。
が挙げられています。
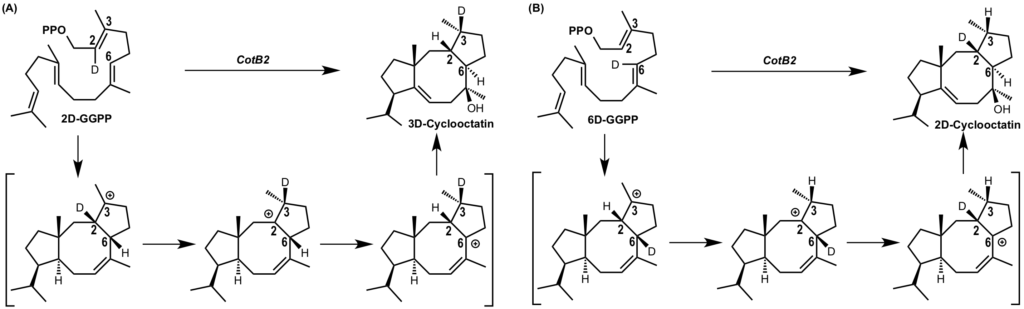
また、図 4 のような重水素標識実験を行うことによって、この計算結果が正しいことが実験科学的にも証明されています(参考文献 1)。
1,5-ヒドリドシフト
1,2-水素移動反応がプロトンシフトということは分かりましたが、他の場合は、どうなのでしょうか?
上述の Cyclooctatin の経路では、1,5-水素移動反応も計算されていますので、それぞれの場合での遷移状態構造を考えてみましょう(図 5)。
プロトンシフトとして考えると、正電荷を帯びているプロトンがカルボカチオンに向かって行くという何ともおかしな反応メカニズムになってしまいます。
となれば、1,5-水素移動反応の場合は、ヒドリドシフトとなるのでしょうか?
ここで実際に DFT 計算を行うと、1,5 水素移動反応の水素は Mulliken charge だとわずかにヒドリドっぽいが、NBO だとわずかにプロトンっぽいという結果になります。まあ、ほぼ中性ということです。
よく分からない計算結果になってしまいましたが、この場合も、遷移状態構造を詳しく見ることで問題は解決できます。
上記の 1,5-水素移動反応では、炭素から炭素へとヒドリドやプロトンが遊離して移動することはありません。
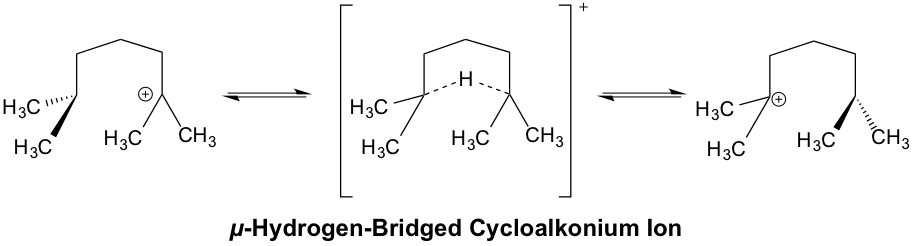
遷移状態では、移動する水素は元々結合していた炭素と移動先の炭素どちらとも近くなっている構造を取っています。
つまり、図 6 に示すような µ-hydrogen bridged Cycloalkonium Ion と見なすことができます(参考文献 2)。
系全体で正の電荷を帯びている非局在化した非古典的カチオン種(ONIUM)であり、プロトンシフトともヒドリドシフトとも言えないような感じです。
なので、やはり1,2-hydrogen shift (1,2-水素移動反応)と呼ぶのが無難な気がします。
1,5-プロトンシフト
しかし、1,5-水素移動反応の場合でも明らかにプロトンシフトの場合もあります。
それは、![]() 電子が関与する場合です(具体例については、下記文献の Fig 1 を参照)。
電子が関与する場合です(具体例については、下記文献の Fig 1 を参照)。
では、どのようにしてプロトンシフトなのかを見分けたら良いのかと疑問に思うかともいると思います。
そのような方には、以下の文献をお勧めします。
“Feasibility of Intramolecular Proton Transfers in Terpene Biosynthesis − Guiding Principles“
Young J. Hong & Dean J. Tantillo*
J. Am. Chem. Soc. 2015, 137, 4134–4140.
DOI: 10.1021/ja512685x
まとめ
1,2–水素移動に関しては、全てプロトンシフトです。その他、1,3-、1,4-、1,5- に関しては、例外も少しあります。
しかし、プロトンシフト(intramolecular proton transfer)という単語はまだ一般的ではないため、使用は避けたほうが良いかもしれません。
無難に 1,2-hydrogen shift、1,2-水素移動反応と呼ぶのが良いかもしれません。
参考文献
- 未解明のテルペン類の生合成経路を理論的に明らかに(Chem Station スポットライトリサーチ)
- “Onium Ions” George A. Olah et al. 1998
- “Feasibility of Intramolecular Proton Transfers in Terpene Biosynthesis − Guiding Principles”
Young J. Hong & Dean J. Tantillo*
J. Am. Chem. Soc. 2015, 137, 4134–4140.
DOI: 10.1021/ja512685x

反応の名称は、反応の本質ではなく、出発物と生成物の構造の変化を示しています。よって、本質ではプロトンシフトの傾向を示していても、ヒドリド移動と命名せざると得ないと思います。芳香族置換反応でも、本質は付加脱離ですが、名称としては置換反応とナルトの一緒だと思います。